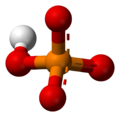
Fosfat
Fosfat, je neorganskoj hemiji so fosforne kiseline. U organskoj hemiji, fosfat, ili organofosfat, je estar fosforne kiseline. Organski fosfati su važni u biohemiji i biogeohemiji ili ekologiji. Neorganiski fosfati se iskopavaju da bi se dobio fosfor za upotrebu u agrikulturi i industriji.[2][3][4] Na povišenim temperaturama u čvrstom stanju, fosfati mogu da se kondenzuju i formiraju pirofosfate.
Hemijske osobine
Fosfatni jon je poliatomski jon sa empirijskom formulom PO43− i molarnom masom od 94.973 g/mol. On se sastoji od jednog centralnog atoma fosfora atom okruženog sa četiri atoma kiseonika u tetraedarskoj konfiguraciji. Fosfatni jon nosi tri negativa formalna naelektrisanja i on je konjugovana baza hidrogen fosfatnog jona, HPO42-, koji je konjugovana baza H2PO4-, dihidrogen fosfatnog jona, koji je konjugovana baza H3PO4, fosforne kiseline. On je hipervalentni molekul (atom fosfora ima 10 elektrona u svojoj valentnoj ljuski). Fosfat je takođe organofosforno jedinjenje sa formulom OP(OR)3.
Fosfatne soli se formiraju kad se pozitivno-naelektrisani jon veže za negativno-naelektrisane atome kiseonika, formirajući jonsko jedinjenje. Mnogi fosfati nisu rastvorni u vodi na standardnoj temperaturi i pritisku. Natrijum, kalijum, rubidijum, cezijum i amonijum fosfati su rastvorni u vodi. Većina drugih fosfata su veoma malo rastvorni ili nerastvorni u vodi. Kao pravilo, hidrogen i dihidrogen fosfati su nešto rastvorniji od korespondirajućih fosfata. Pirofosfati su uglavnom rastvorni u vodi.
U razređenim vodenim rastvorima, fosfat postoji u četiri oblika. U jako-baznoj sredini, fosfatni jon (PO43−) predominira, dok u slabo-baznim uslovima, hidrogen fosfatni jon (HPO42−) je prevalentan. U slabo-kiselim uslovima, dihidrogen fosfatni jon (H2PO4−) je najzastupljeniji. U jako-kiseloj sredini, fosforna kiselina (H3PO4) je glavna forma.
-
H3PO4 -
H2PO4− -
HPO42− -
PO43−
Precizniji, polazeći od sledeće tri ravnotežne reakcije:
- H3PO4 Šablon:Eqm H+ + H2PO4−
- H2PO4− Šablon:Eqm H+ + HPO42−
- HPO42− Šablon:Eqm H+ + PO43−
korespondirajuće konstante disocijacije na 25 °C (u mol/L) su:
- (pKa1 2.12)
- (pKa2 7.21)
- (pKa3 12.67)
Literatura
Šablon:Reflist Šablon:- Šablon:Jedinjenja fosfora-lat Šablon:Commonscat